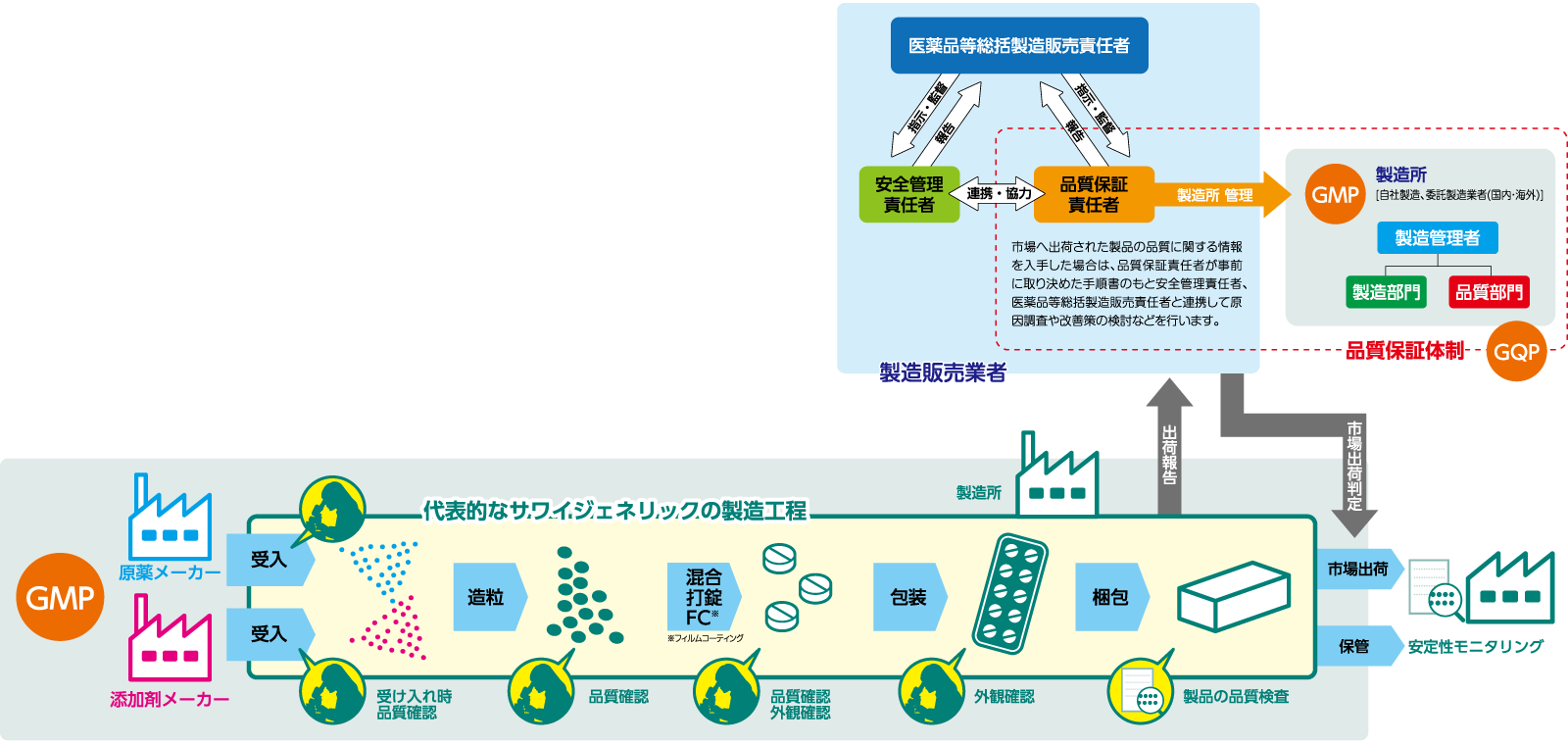
サワイジェネリックにおける“品質管理体制”
医薬品製造におけるGMPの適用範囲は非常に多岐にわたります。具体的には、原材料の受け入れから始まり、製造、試験、保管、そして最終的に製品が市場に出荷されるまでの全ての一連の工程に及びます。この徹底した管理は、医薬品の品質を保証し、患者さんへ常に安定して医薬品を供給し続けるために不可欠です。
GMPの遵守状況は、GQPに基づき、製造販売業者が責任を持って管理・監督しています。これには、市場への出荷管理、その記録作成の手順などが含まれ、製造販売業者は市場に出荷される製品の品質に全責任を負います。これにより、高品質な医薬品が継続的に市場に提供される体制が維持されます。
さらに、医薬品製造企業は規制当局や都道府県の薬務主管課から定期的なGMP適合性調査を受けます。これは、法令遵守のもとで製造管理が適切に行われているかを確認するための重要なプロセスです。これらの厳格な管理体制を通じて、医薬品の品質と安全性が確保され、ひいては患者さんへの安定供給が実現されています。
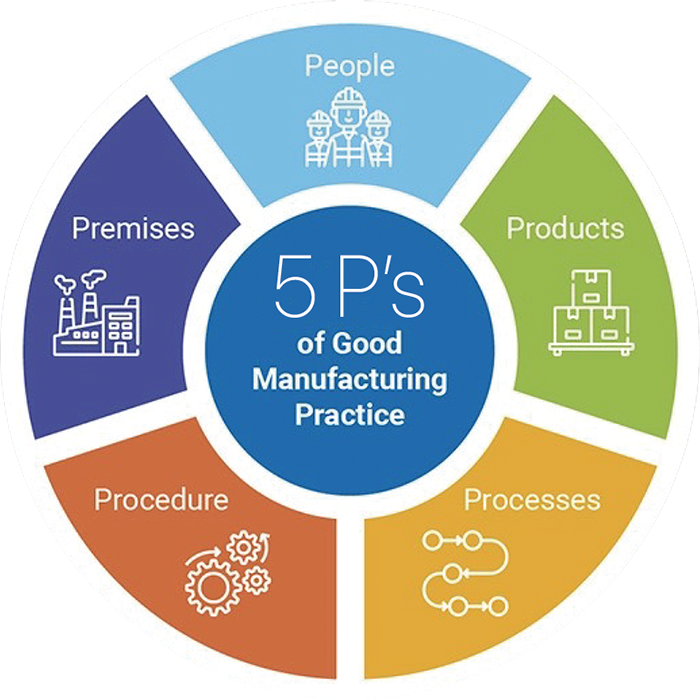
「医薬品及び医薬部外品の製造管理及び品質管理の基準」(Good Manufacturing Practice)のことであり、医薬品等の製造業者(海外製造所を含む)が遵守すべき品質管理基準です。基本的な考えとして以下の3つ(三原則)があります。
- 原則1:
- 人為的な誤りを最小限にすること
- 原則2:
- 医薬品の汚染及び品質低下を防止すること
- 原則3:
- 高い品質を保証するシステムを設計すること
製造販売業者に求められる「医薬品等の品質管理の基準」(Good Quality Practice)のことです。製造販売業者が行うべき具体的な品質管理業務が定められています。主な内容は以下の通りです。
- 医薬品等総括製造販売責任者の監督の下、医薬品の品質管理業務を統括する責任者として、「品質保証責任者」の設置
- 品質管理業務を適正かつ円滑に行うための手順書の作成・運用
- 市場への医薬品出荷の管理
- 製造業者(海外製造所を含む)との製造管理や品質管理に関する取り決め
- 医薬品の品質情報(ご指摘等)を得た際の情報評価、原因究明及び改善措置
- 品質不良が生じた際の回収等を含めた危害発生防止措置
拡大して見る
閉じる
原薬の「ひとつ上の品質」を目指した“サワイスペック”
「ひとつ上の品質」にこだわり、原薬によっては、承認規格より厳しい自主基準(サワイスペック)を設定し、適合したもののみを使用しています。原薬サンプルは世界中から収集し、性状、溶状など多くの項目の品質評価を行っています。特に、純度試験を重視し、類縁物質測定などを多角的に評価しています。
その中で当社製品の特性に最も適している原薬について、原薬製造所の製造設備、薬事対応力、持続的な安定供給能力を吟味して選んでいます。
“ニトロソアミン類”の発生リスク評価
当社では新しい概念として、添加剤などに含まれる窒素酸化物などのニトロソ化剤(NOx)のうち、実際にニトロソ化に寄与するNOxを「反応性NOx」と定義し、その量によりニトロソアミン類の発生リスクを定量化する試みを行っています(NOXANA®)。また、製品の品質を満たしながらニトロソアミンの生成を抑える複数の添加剤を発見しました(SUPRENA®)。これら技術によりニトロソアミンを抑えた製剤設計が可能となりました。
“サワイスペック”の品質管理
製品を市場に出荷する際の品質確認だけでなく、製品の製造工程の各所で品質チェックを行い、最終製品が高品質となるよう慎重に製造しています。さらに当社では、原薬のロットの違いや季節変動による造粒状態の変化に対し、徐放性製剤などの特殊な製剤は製造前に試打して一定の基準内の品質が確保されていることを確認しています。
市場出荷後も高品質な製品が患者さんに届いているかを確認するために、有効期間を超える期間の品質確認(安定性モニタリング)を実施する等、品質確保に努めています。
品質保証体制の強化
工場における第三者チェックは、これまでは工場の品質保証部が行う自己点検のみでしたが、医薬品製造管理者直轄となる現場QAを新設しました。医薬品製造管理者が製造部門及び品質部門を適切に監督するとともに、製造部門及び品質部門の業務が適切かつ円滑に行われる体制を整備し、さらに強固な品質保証体制を構築しています。
また、全工場の製造エリア、保管エリア等に監視カメラを設置して作業の透明性強化を図っています。

データインテグリティ(文書及び記録の信頼性の確保)の推進
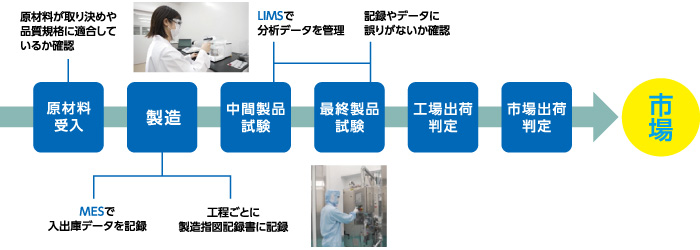
製品の品質は、製品そのものだけでなく、試験データが適切に管理・保管されていることで担保されます。そこでデータ管理システムとしてMESやLIMSを導入し、可能な限り人が介在しないシステムを構築することにより、製造した製品の品質をより厳密に確保することが可能になると考えています。すでに一部の工場では導入し、運用を開始しています。 MESとLIMSが連携することで、製造工程全体を通じて品質を保証し、規制要件を遵守した効率的な医薬品製造が実現できます。また、逸脱が発生した場合や製造方法、試験方法を変更する場合、担当者から責任者へ報告・申請が遅滞なく上がり、関連部署へ情報が速やかに共有される品質イベント管理システムを構築しています。
製造工程の把握や管理、作業者への指示や支援などを行う「製造実行システム」(Manufacturing Execution System)のことです。原材料(原薬・添加剤・包材)及び工程ごとの中間製品をID管理し、製造工程中に不備が発生すると、次の工程に進めないようにシステム的にロックがかかります。 適合をもって初めてロック解除され、次工程に進む仕組みです。また、原材料及び中間製品の在庫管理は、それぞれの工程ごとに原材料に貼られたバーコードを読み込んでシステムで照合及び所要量を投入するため、誤って別の原材料や中間製品が使用されたり、過不足が発生することを防止します。 システムによって管理されているため、人による改ざんや誤記入がなく、製造工程における原材料や中間製品の仕込み間違えや数量の人為的な誤りを抑えることが可能となります。
ネットワークを介して分析結果が分析機器から直接システムに入力されるなど、試験業務を統合管理するシステムのことです(ラボラトリー情報管理システム;Laboratory Information Management System)。試験の開始時に検体や試薬、試験機器に貼付されたバーコードを読み取り、自動でデータ収集をするため、人による改ざん及び誤記入を防ぐことができます。 また、試験操作及びデータの一連のすべての情報を一元的にデジタル管理することで、業務の効率化、ヒューマンエラーの削減、トレーサビリティの確保などを実現します。
拡大して見る
閉じる
GMP教育
当社では、全従業員に薬機法およびGMPの基礎教育を実施しておりますが、生産本部の従業員に対しては、さらに実務的なGMP教育を行うべく、eラーニング講座を開設するなどの研修体制を構築しました。また、研修実施の効果を定量的に評価できるよう、確認試験も実施しています。
(2025年9月作成)