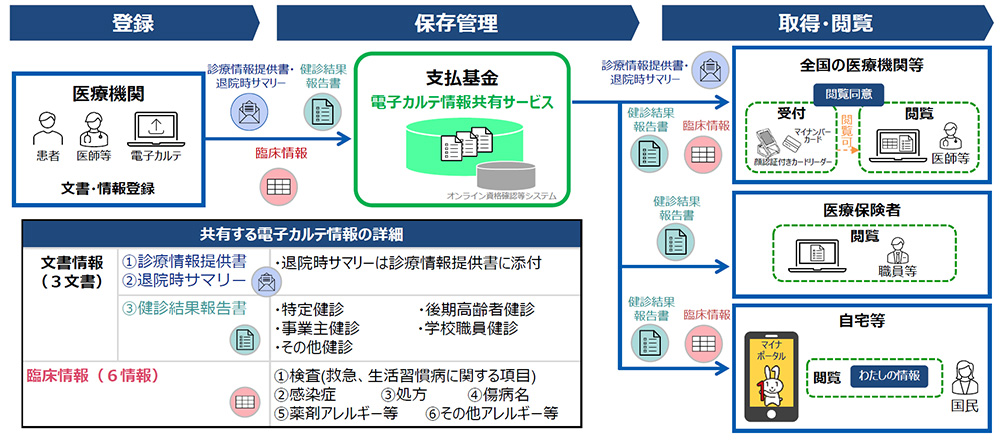
中央社会保険医療評議会総会は12月26日、2026年度薬価制度改革の骨子を決定、薬価算定基準等の改正案に反映され、1月16日に了承されました。長期収載品の薬価の更なる適正化やオーソライズド・ジェネリック(AG)の新薬収載時の薬価見直しなどが改正案に盛り込まれました。以下で主な内容を見ていくことにしましょう。
■長期収載品の段階的薬価引き下げをG1に一本化、適用時期を後発品上市から5年後に前倒し
長期収載品では、後発品の上市後5年と10年のタイミングで後発品への置換え率に応じて薬価を段階的に引き下げるルールの大幅な見直しが行われます。
後発品上市から10年経過後に適用されるルールには、▽後発品置換え率が80%以上の品目が対象のG1、▽置換え率80%未満の品目が対象のG2、▽すでに薬価が一定程度下がっているためにG1、G2の対象にならない品目の補完的引き下げルールのC-の3種類がありますが、これをG1に一本化。適用時期も前倒しし、後発品上市から5年経過した長期収載品は後発品置換え率を問わず、G1が適用されることになります(図表1)。
【図表1】長期収載品の薬価の更なる適正化(イメージ)
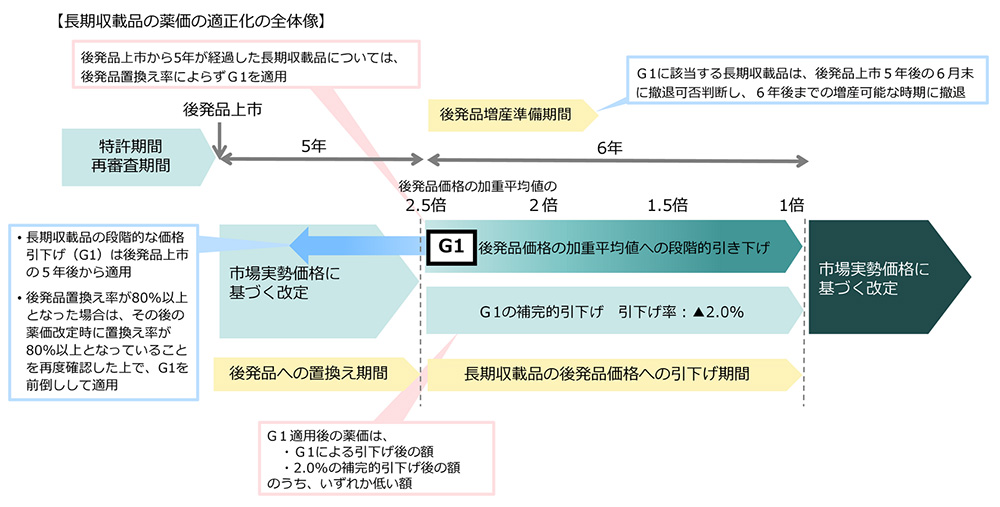
出典:薬-2 令和8年度薬価改定について⑦(令和7年12月3日 中央社会保険医療協議会薬価専門部会(第242回)), https://www.mhlw.go.jp/stf/newpage_66593.html より作成
さらに従来のCに代わる薬価の補完的引き下げルールを設けます。引き下げ率は後発品置換え率に関係なく一律2%とし、G1適用後の薬価には、G1による引き下げ後の額と補完的引き下げ後の額のうち、いずれか低い額を適用します。
これらの見直しに伴い、これまでの後発品上市5年後の引き下げルールであるZ2は廃止。バイオ後続品(バイオシミラー)のあるバイオ先行品に新たにG1を適用することも決まりました。
今改定における2024年度の薬価改定時にG2に該当していた品目の取り扱いは、下記の通りです(図表2)。
▽初めてG2に該当または該当から2年経過していた品目
G1該当から2年後の区分を適用し、後発品薬価の加重平均値の2倍まで薬価を引き下げ
▽G2該当から4年または6年経過していた品目
G1該当から4年後の区分を適用し、後発品薬価の加重平均値の1.5倍まで薬価を引き下げ
なお、長期収載品の関連では選定療養における追加負担水準の見直しも併せて実施。これまでの後発品との価格差の1/4相当から1/2相当に引き上げます。
【図表2】2024年度薬価改定時にG2に該当した品目の取り扱い
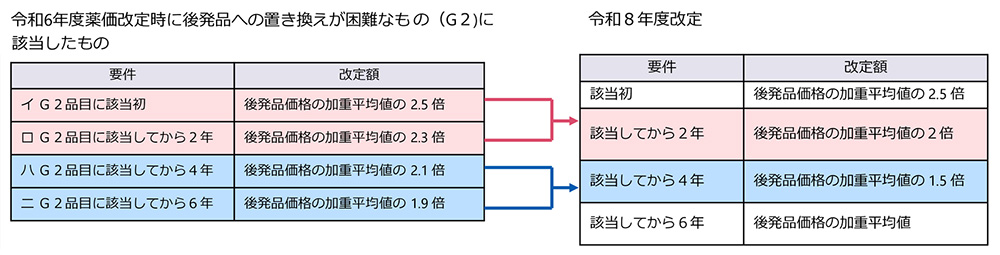
出典:薬-2 令和8年度薬価改定について⑦(令和7年12月3日 中央社会保険医療協議会薬価専門部会(第242回)), https://www.mhlw.go.jp/stf/newpage_66593.html より作成
■AG・バイオAGの新規収載時の薬価は先発品と同額とし、後発品との適切な競争促す
これまでは新規後発品の薬価はAGも含め、原則として先発品の薬価に0.5を乗じた額に設定されていました。ただ、AGは後発品よりも市場シェアが大きくなる傾向がある上、先発品企業がAGの製造販売業者からライセンス料を得るケースが多いことから、「形を変えた先発品企業の長期収載品依存になっている」との意見もありました。
そこで2026年度制度改革では後発品の適切な競争環境の形成・維持を目指し、AGの新規収載時の薬価を先発品と同額とする見直しを行います。バイオAGの新規収載時の薬価もバイオシミラーと同一の扱い(=バイオ先行品の薬価の0.7掛け)を改め、先行品と同額とします。なお、このルールは2026年10月以降に薬価収載されたものから適用されます。
■後発品の価格帯集約ルール、A区分企業の品目は価格集約せず銘柄別改定
後発品を中心とした医薬品の安定供給確保のための対応として後発品の価格帯集約ルールに関しては、▽注射薬とバイオシミラーは同一規格・剤形内の品目数が少なくなっていることを踏まえ、最高価格の30%を下回る薬価のものを除き、価格帯集約を行わない、▽G1品目の後発品の1価格帯集約は廃止する、▽企業指標による評価でA区分となった企業の対象品目、適用条件のいずれの要件も満たす品目は価格帯集約をせず、品目ごとの改定とするー見直しを行います(図表3)。
【図表3】後発品の価格帯集約 見直し後の適用イメージ
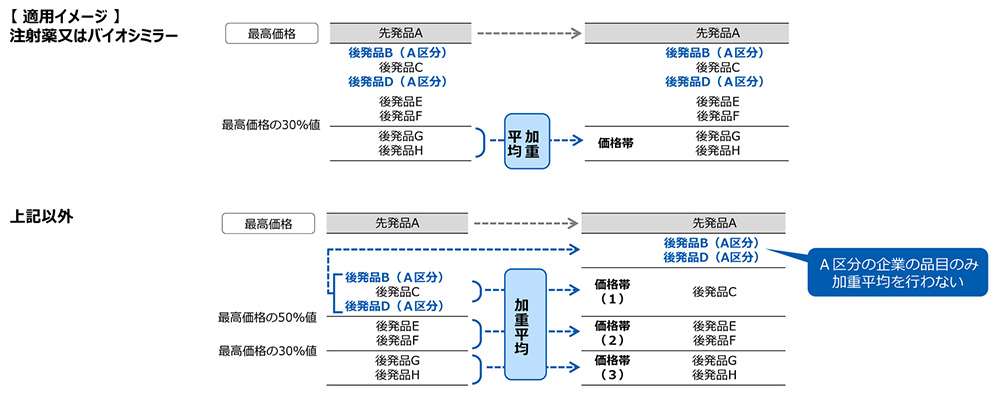
出典:薬-2 令和8年度薬価改定について⑦(令和7年12月3日 中央社会保険医療協議会薬価専門部会(第242回)), https://www.mhlw.go.jp/stf/newpage_66593.html より作成
■薬価の下支え制度の充実、最低薬価・不採算品再算定
最低薬価では、局方品で錠・カプセルなどが10.80円/錠・Cap、散剤(細粒剤を含む)・顆粒剤などが8.00円/g等、その他の医薬品で錠・カプセルなどが6.30円/錠・Cap、散剤(細粒剤を含む)・顆粒剤などが6.90円/gなど、一律3.5%を引き上げます。外用塗布剤は規格単位に応じた最低薬価の区分に新たに加える他、点眼・点鼻・点耳液には、点眼薬の最低薬価を適用します。
不採算品再算定は、▽基礎的医薬品とされたものと組成及び剤形区分が同一の品目、▽重要供給確保医薬品に位置付けられている品目、▽極めて長い使用経験があり供給不足による医療現場への影響が大きいと考えられるその他品目など、継続的な確保を特に要する薬剤であって、特定の企業からの供給が途絶えた時に代替供給の確保が困難な品目-のいずれかを満たす品目を対象に実施します。
また、組成、剤形区分及び規格が同一の類似薬が全て不採算品に該当することを求める要件は廃止し、該当する類似薬のシェアが5割以上であって他の要件を満たす場合は不採算品再算定を適用する取り扱いに改めます。
■新薬創出等加算は制度の趣旨明確化のため名称変更、市場拡大再算定の共連れルールは廃止へ
この他にも、▽「新薬創出・適応外薬解消等促進加算」は「革新的新薬薬価維持制度」に名称変更、▽市場拡大再算定の類似品への適用(いわゆる共連れルール)の廃止、▽市場が急拡大した高額医薬品の再算定における薬価引き下げ幅の拡大-などが実施されます。